eCTD 管理電子送件解決方案:EXTEDO eCTDmanager - 訊聯基因
eCTD是什麼?
eCTD (electronic Common Technical Document,電子化通用技術文件) 由 ICH 2003 年公告後,美國、歐盟、日本、加拿大等國已規定藥品技術性資料須以 eCTD 送件,中國亦積極規畫 eCTD 送件規範,以提升藥品送件及審查的效率與管 理。新藥公司進行新藥研發,研擬法規策略及國際佈局,須積極了解各國 eCTD 之 管理法規及送件實務。
訊聯基因數位(GGA, 原名:創源生技)分子數位中心有感於電子化的浪潮,在藥物電子送件領域深耕多年, 現代理 EXTEDO 相關送件軟體,提供專業的教育訓練與軟體的建置和維護, 讓客戶快速上手,並協助解 決客戶全球送件問題, 使客戶在紙本銜接電子化的歷程更加順利。 近年並承接 TFDA 藥物查驗系 統的建置,結合法規及資訊專家,在電子送件議題上擔任政府協力者的角色。
eCTDmanager – eCTD管理電子送件解決方案
eCTDmanager受到全球超過35個國家監管機構所信任,eCTDmanager完全符合ICH和區域的送審規範,可以使您輕鬆地在全球進行送件。透過eCTDmanager您可以建立、審閱、驗證和發佈基於eCTD、NeeS、eCopy、IMPD、CTA、MAA、VNeeS、DMF、ASMF及其他送審格式的申請。
有效驗證和合規的電子送件是一個複雜的過程。依據標準送審格式來建立、審查、驗證和發佈,這伴隨著一系列的挑戰。此外,面臨多個區域的送審管理不僅要符合ICH的規範,還要符合地區規範,這使整個送審過程更加複雜。
為了電子送件的合規性,您需要一款eCTD軟體解決方案,它能夠協助您在多個地區市場針對不同產品全面了解您的送審狀態。EXTEDO eCTDmanage旨在滿足您的這些需求,確保您輕鬆符合各項法規要求。
eCTDmanager提供完整的監管檔案管理和解決方案。它的可擴充性及整合所有送審管理功能於一身,能滿足您電子送件及紙件送件的要求。直觀的操作介面簡單易上手,導入的word文檔將自動轉換成PDF格式,使您能夠輕鬆地處理電子送件。
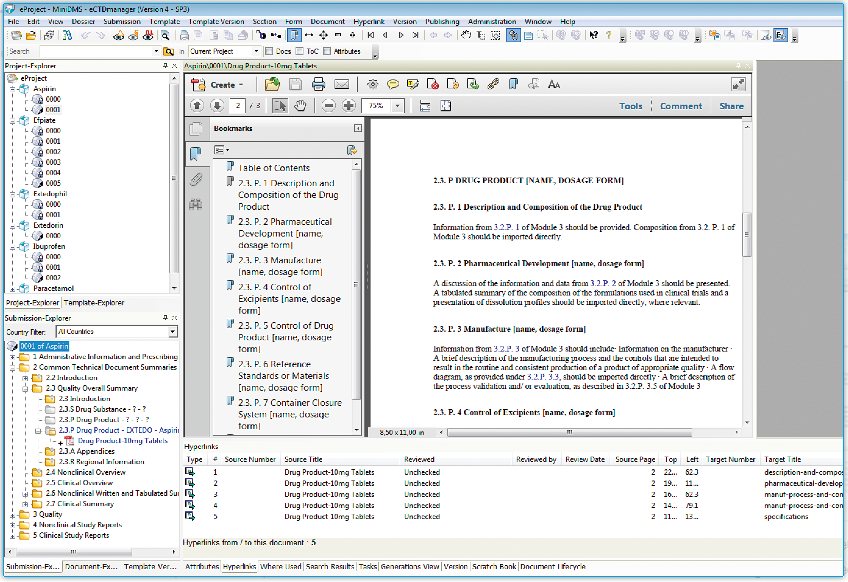
eCTDmanager的優勢:
- 快速符合全球最新的監管法規變化
- 可以針對單一申請,驗證及發佈其送審
- 支持世界上所有地區的結構和格式申請的發佈
- 提高送件的品質和一致性
- 先進的超連結和書籤應用
- 符合ICH和地區性檔名和21 CFR Part 11。
- 最低的硬體要求,高效能
- 快速系統部屬及系統驗證
- 少量訓練即可上手使用
聯絡我們



